
本文阅读时长约 6分钟,共 2350字。
【引言】
嵌合抗原受体(chimeric antigen receptor,CAR)T细胞疗法是一种利用患者自身免疫系统治疗癌症的新型治疗方法。
CAR-T细胞通过重定向T细胞应答,使其针对特异性肿瘤抗原,克服了以往T细胞免疫治疗的局限性。同时,CAR能够以主要组织相容性复合物非依赖性方式识别抗原,使其能够靶向更多类型的抗原。
CAR-T细胞疗法的开发和应用为众多肿瘤患者带来了新的治疗希望。那么,CAR-T细胞如何获得,又如何发挥治疗作用呢?接下来,就让我们一起来了解一下吧!

CAR通常由胞外靶向结构域、跨膜间隔区和胞内信号域组成(图1)。CAR的靶向结构域通常来源于抗体的抗原结合区域,即形成抗体结合位点的免疫球蛋白重链和轻链。CAR的胞内结构域包含CD3ζ链,为基因修饰的T细胞提供T细胞受体活化信号和增殖刺激。CAR结构的设计影响CAR-T细胞的增殖和存续动力学等药代动力学特征,从而影响其有效性和安全性。第一代CAR的胞内信号域由T细胞受体(T cell receptor,TCR)信号域(TCRξ链)组成,增殖反应较差,细胞毒性较低,导致抗肿瘤疗效差,且只能产生短暂的T细胞应答,不能诱导持久的肿瘤缓解。为了提高第一代CAR的疗效,第二代CAR的胞内结构域除了包含TCRξ链外,还包含一个CD28或4-1BB共刺激信号结构域,CD28结构域增强了CAR-T细胞的初始活化和增殖并改善了效应功能,而4-1BB结构域主要改善了CAR-T细胞的扩增和长期存续性。目前美国食品药品监督管理局批准的商业化CAR-T细胞均为第二代CAR(表1):Tisagenlecleucel、Axicabtagene ciloleucel、Brexucabtagene autoleucel、Lisocabtagene maraleucel和Idecabtagene vicleucel。同时大量的研究正集中于新一代CAR的设计,以进一步增强CAR-T细胞的疗效和安全性。
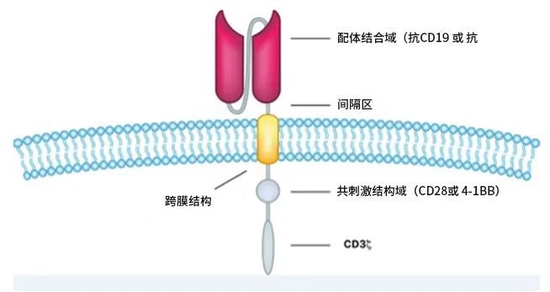 图1.CAR的结构
图1.CAR的结构  表1.美国食品药品监督管理局批准的CAR-T细胞产品
表1.美国食品药品监督管理局批准的CAR-T细胞产品注释:ALL,急性淋巴细胞白血病;BCL,B细胞淋巴瘤;BMCA,B细胞成熟抗原;DLBCL,弥漫性大B细胞淋巴瘤;FL,滤泡性淋巴瘤;MCL,套细胞淋巴瘤;PMBCL,原发性纵隔B细胞淋巴瘤;R/R,复发/难治性。
a 制备所需时间来自关键注册试验或生产商文件中报告的时间。在实际应用中,该时间可能有较大差异。
CAR-T细胞治疗时,首先需要通过白细胞单采术采集癌症患者的T细胞,随后将其运送至中心生产机构进行基因工程改造,以表达识别肿瘤相关靶抗原的CAR。经过体外扩增后,将CAR-T细胞回输至患者体内,在理想情况下,回输的CAR-T细胞将识别靶抗原,增殖并攻击肿瘤细胞,最终使得肿瘤缓解。从白细胞采集到回输的这一时间段称为“静脉至静脉时间”,通常约为3周,在此期间疾病必须维持稳定,而这给进展较快的患者带来了挑战。为了在CAR-T细胞回输前控制疾病,必须进行桥接治疗,即使用化疗或放疗,以在CAR-T细胞回输前控制疾病,然而桥接治疗很可能导致毒性和感染,使患者不适合接受包括CAR-T细胞治疗在内的进一步治疗。回顾性分析显示,需要桥接治疗的患者进行CAR-T治疗的预后也更差。此外,为了降低CAR-T细胞排斥反应的风险并促进CAR-T细胞增殖,患者需在CAR-T细胞回输前接受淋巴细胞耗竭化疗。
目前,CAR-T细胞疗法仅适用于疾病多次复发的癌症重症患者。既往认为该类患者的预后较差,但如今已有了较大的改善。CAR-T细胞疗法在急性淋巴细胞白血病(acute lymphoblastic leukemia,ALL)、淋巴瘤和多发性骨髓瘤患者中显示出了显著且持久的缓解:复发/难治性B细胞ALL患者接受CAR-T细胞治疗后的缓解率约为80%-90%,中位总生存期超过1年;淋巴瘤患者接受CAR-T细胞治疗的总缓解率和完全缓解率分别在50%-80%和40%-60%;部分ALL患者和淋巴瘤患者可获得多年的缓解。

然而与其他癌症治疗方法一样,CAR-T细胞疗法虽具有高度缓解、长期缓解和治愈的可能,但同时也可能发生严重、可能危及生命但可逆的副作用。约10%-30%的患者在接受CAR-T治疗后将出现严重毒性和重度器官功能障碍,这些患者中有很大一部分将需要入住重症监护病房(intensive care unit,ICU)并接受生命支持措施(如灌注引导的液体治疗、血管活性药物、有创或无创机械通气或肾脏替代治疗)。值得庆幸的是,如果能够及时给予适当的管理,需要收住ICU的患者结局将相对良好。因此,在安全、有效地向癌症患者提供免疫效应细胞治疗的临床管理框架中,重症监护是重要的组成部分。
内容编辑:小聚
【参考文献】
1.Shimabukuro-Vornhagen A, Böll B, Schellongowski P, et al. Critical care management of chimeric antigen receptor T-cell therapy recipients. CA Cancer J Clin. 2022, 72(1):78-93. doi: 10.3322/caac.21702.
【版权说明】
本文由《聚焦CA》整理发布,编辑/排版:小聚;文中图片来源:CA、聚焦CA设计图。本资料为仅用于学术会议或活动的专业资料,旨在促进医药信息的沟通和交流,仅供医疗卫生专业人士参考。转载请保留以上完整出处,文章版权归原作者所有。如有版权问题或商讨其他合作请后台联系邮箱:focusca@yingmingcg.com。


 美摄影师为患病儿童拍超级英雄照
美摄影师为患病儿童拍超级英雄照 海南黎族文身即将消失
海南黎族文身即将消失 哪些人容易得慢阻肺
哪些人容易得慢阻肺 正常人如何预防脑出血
正常人如何预防脑出血 仁心在左 责任在右
仁心在左 责任在右 推己及人 以达极致
推己及人 以达极致 草莓吃腻了?这些吃法你肯定没试过!
草莓吃腻了?这些吃法你肯定没试过! 与癌共存:食管癌病人的自述
与癌共存:食管癌病人的自述 香味浓郁猪肉松
香味浓郁猪肉松 唐朝吉祥菜四喜丸子
唐朝吉祥菜四喜丸子 练起来!全身都要瘦!
练起来!全身都要瘦! 缓解痛经的九款药膳
缓解痛经的九款药膳